Más Información

Fiscalía de Tamaulipas dio contratos a empresa sancionada por EU; destina 1 millón 200 mil pesos a módulos LED y pantalla

Familia pernocta afuera de su casa por afecciones tras fuga de agua en Álvaro Obregón; "mi patrimonio se redujo a basura"

Expertos ven a Infodemia MX como un órgano de propaganda y sin metodología de verificación; 6 de cada 10 “desmentidos” en 2025 están vinculados a la 4T

Andrea Chávez pide licencia; "dejo el Senado para atender la tarea de acabar con 100 años de PRIAN en Chihuahua"

"No hay triunfos para siempre, Verde no debe confiarse": Monreal; reacciona a ruptura de coalición con Morena en SLP

Buscaré la candidatura de Guerrero solo si Morena me lo pide: Félix Salgado; "voy si el partido me dice que le falta un lucero", dice

PAN Puebla definirá candidaturas 2027 con encuestas y consulta; habrá apertura para perfiles ciudadanos

PVEM se prepara para ir solo en CDMX en elecciones de 2027; no hay comunicación con Morena, afirma Jesús Sesma
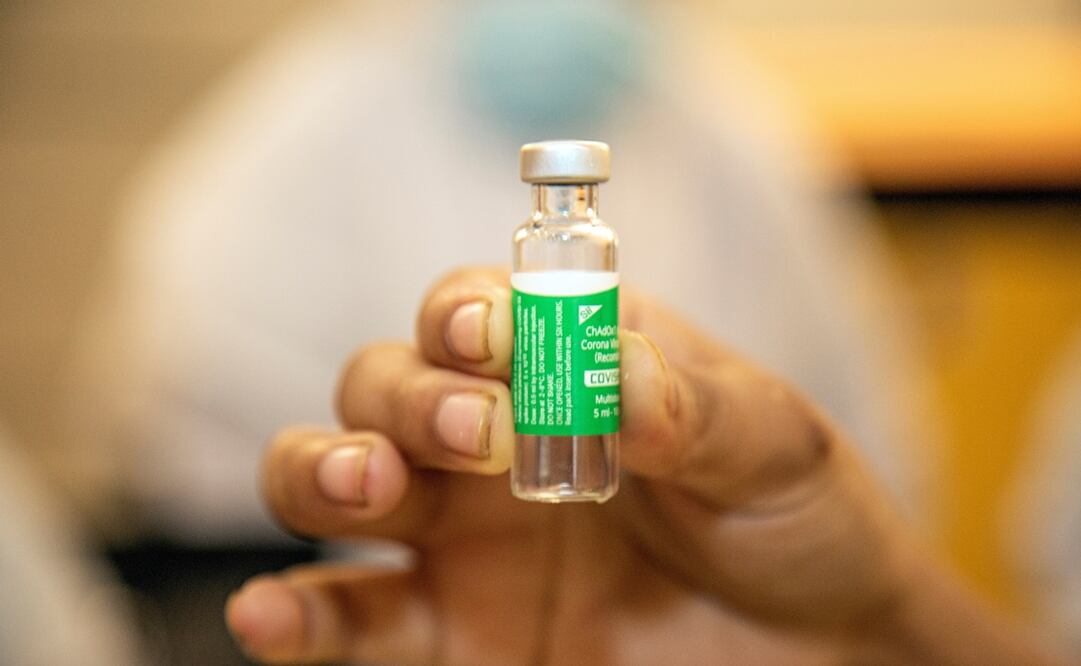
Londres.- La farmacéutica AstraZeneca anunció este domingo que ha comenzado un estudio clínico de fase II/III para evaluar la seguridad y la respuesta inmune que genera una nueva versión de su vacuna contra el Coronavirus adaptada a la variante Beta , identificada por primera vez en Suráfrica (B.1.351).
La multinacional británicosueca informó en un comunicado que hoy recibieron la primera dosis de esa nueva vacuna, denominada AZD2816, los primeros participantes en un estudio para el que se reclutarán aproximadamente 2 mil 250 adultos en el Reino Unido, Suráfrica, Brasil y Polonia.
El preparado se administrará a individuos que previamente ya habían recibido la de Vaxzevria -la vacuna original de AstraZeneca- o bien de una vacuna que utilice tecnología de ARN mensajero (mRNA), como las de Pfizer y Moderna.
La nueva versión se inoculará al menos tres meses después de haber recibido la última dosis de la primera vacuna. En caso de personas no inmunizadas previamente, se administrará en dos dosis, separadas por un intervalo de cuatro o bien doce semanas.
También se inoculará la versión AZD2816 como segunda dosis cuatro semanas después de una primera inyección de la versión original de Vaxzevria.
Lee también:
La vacuna que se somete a prueba ha sido diseñada utilizando el mismo vector adenoviral que la anterior, con "alteraciones genéticas menores en la proteína espicular basadas en la variante beta (B.1.351)", detalló la firma.
Esta versión de la vacuna contra el SARS-CoV-2 contiene diez cambios en la proteína espicular, muchos de los cuales no solo se encuentran en esa variante, sino también en otras con efectos "preocupantes".
Entre ellos, reducen la capacidad de los anticuerpos inducidos por la vacuna para bloquear la entrada del virus en las células (mutaciones K417N, E484K y N501Y); incrementan la transmisibilidad del virus (D614G) y reducen la sensibilidad de los anticuerpos (L452R).
"Es importante que nos mantengamos por delante de las variantes genéticamente distintas del coronavirus. (La vacuna) AZD2816 debería ayudar a ampliar la respuesta inmune de los individuos contra la emergencia de variantes preocupantes", indicó el vicepresidente ejecutivo de I+D de AstraZeneca, Mene Pangalos.
El director del Grupo de Vacunas de Oxford, que participa en la investigación, destacó por su parte que "poner a prueba las dosis de refuerzo de vacunas existentes y las vacunas para nuevas variantes es importante para asegurarnos de que estamos bien preparados para mantenernos por delante de la pandemia".
Lee también:
afcl
Más Información
Noticias según tus intereses
ViveUSA
[Publicidad]